1) Histoire des modèles de l'atome
Un modèle est un "outil" Un modèle scientifique est toujours provisoire. En effet, au fil des découvertes et des
perfectionnements de l'instrumentation, un nouveau modèle devient nécessaire lorsque les faits ne peuvent être
expliqués avec l'ancienne théorie.
2) La matière est constituée à partir d’atomes
Tous les corps sont constitués à partir de particules infiniment petites
:
les atomes.
Un atome est constitué d’un noyau et d’un nuage d'électrons qui gravitent
autour de lui.
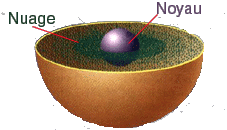
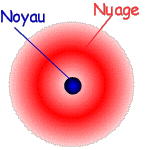
Un électron est une particule chargée d’électricité négative.
Symbole e-.
On l’appelle charge électrique élémentaire
Tous les électrons sont identiques quelque soit l’atome dont ils
proviennent.
électriquement neutres et des protons chargés positivement
Un atome est électriquement neutre car il possède autant de charges positives
dans son noyau que d’électrons.
Le noyau est environ 100 000 fois plus petit que l’atome mais sa masse vaut plusieurs milliers
de fois celle des électrons.
L'atome est formé essentiellement de vide, on dit qu'il a une structure lacunaire
Ordre
de grandeur des dimensions d’un atome
1°
partie : Votre idée sur la taille d’un atome
Indiquez
votre idée sur la feuille
Travail
à faire par groupe de 4
Vous avez 5 min pour vous mettre d’accord sur l’estimation de la taille d’un atome. Indiquez votre estimation
dans le rectangle et
rendez-le au professeur
2°
partie : L’atome d’or
Travail à faire individuellement
Doc. 2 : l'atome d'or
 |
Répondez aux questions suivantes en utilisant les fig 1
et 2 de votre livre p 38
1. Comment les atomes sont-ils disposés dans l'or (comme dans tous les métaux) ? 2. Peux-tu mesurer avec précision le diamètre apparent d'un atome sur la figure ? Explique. Mesure quand même le diamètre d'un atome sur la photo. 3. Mesure la place occupée par 10 atomes sur la photo.
4. Explique pourquoi c'est mieux de faire la mesure
pour 10 atomes que pour 1. 5. Déduis le diamètre d'un atome sur la photo. Convertis-le en mm. vérifie que l'incertitude est |
devenue assez faible, et compare ton résultat à
la 1ère mesure.
6. Est-ce le diamètre réel d'un atome d'or ?
Explique.
7. Convertis ton diamètre en m. Sachant que le microscope grossit l'image 13 millions de fois, calcule le diamètre
réel d'un atome d'or (en m).
Les dimensions d’un atome sont de l’ordre de 0, 1 nanomètre. 1 nm =
10-9
m.
3) Classification périodique des atomes
Chaque type d’atome possède un nombre déterminé d’électron que l’on appelle numéro
atomique symbole Z.
Mendeleïev a classé les atomes par nombre croissant d’électrons.
C’est la classification périodique des atomes .

L’atome de fer possède 26 électrons et 26 charges + dans son noyau.
positive dans son noyau
4) Le noyau d'un atome peut-il subir des transformations

Conclusion
Exercices

Compléter Source: Bordas coll Regaud Vento



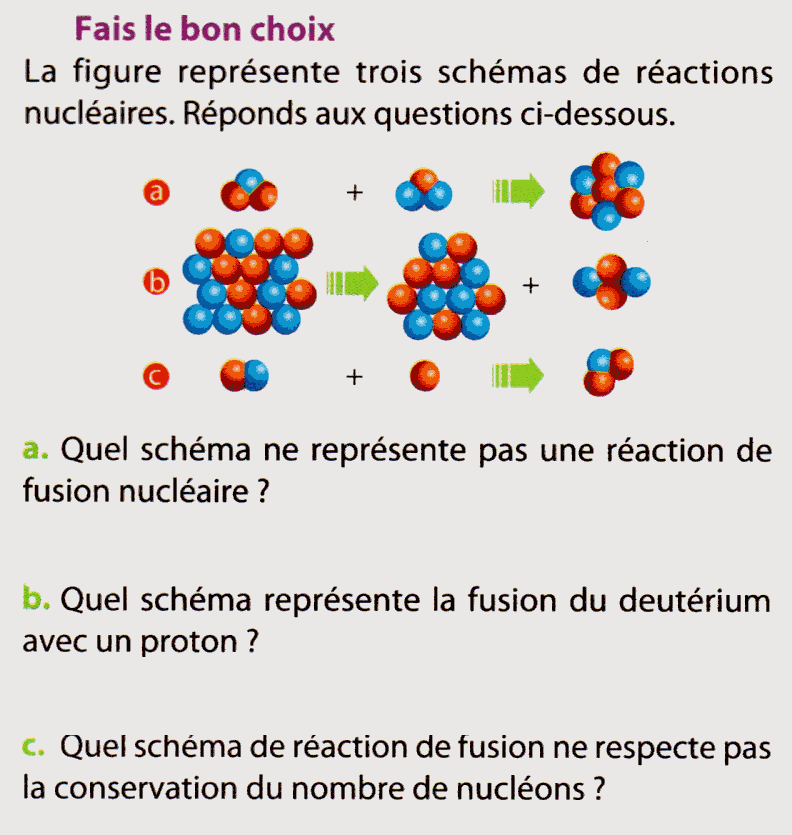
Source: Bordas coll Regaud Vento