1)Etude de document


Les réactifs de la réaction acide chlorhydrique-soude sont l'acide chlorhydrique (H+ + Cl-) et la soude (Na+ + OH-) Les produits sont l'eau (H2O ) et le chlorure de sodium (Na++ Cl-)
Les réactifs de la réaction acide chlorhydrique-fer sont l'acide chlorhydrique (H+ + Cl-) et le fer (Fe) Les produits sont le dihydrogène (H2 ) et le chlorure de fer (Fe2++ 2Cl-)
Dans la première équation de réaction il y a 2 atomes d'hydrogène et un atome d'oxygène dans les réactifs comme dans les produits. Il y conservation des atomes au cours de la transformation chimique
Dans la deuxième équation de réaction il y a 2 atomes d'hydrogène et un atome de fer dans les réactifs comme dans les produits. Il y conservation des atomes au cours de la transformation chimique
Les espèces spectatrices ne sont pas modifiées au cours d'une transformation chimique.
Dans la première équation de réaction Le nombre total de charges est nul dans les produits comme dans les réactifs
Dans la première équation de réaction Le nombre total de charges est +2 dans les produits comme dans les réactifs
Le nombre total de charges est le même dans les produits que dans les réactifs
Conclusion
Lors de l'action de l'acide chlorhydrique avec la soude, l'ion hydrogène de l'acide réagit avec l'ion hydroxyde de la base pour former de l'eau
Lors d'une réaction entre un acide et un métal, l'ion hydrogène de l'acide réagit avec le métal pour former du dihydrogène et un ion métallique.
L'acide chlorhydrique réagit avec le zinc, le fer, l'aluminium mais pas avec le cuivre, l'or ou l'argent
Une transformation chimique conserve le nombre de charges total, la nature et le nombre des atomes
2)Une transformation chimique peux produire de la chaleur
Lors de la réaction entre l'acide et la soude la température du mélange réactionnel augmente
Une transformation chimique peut libérer de l'énergie thermique.
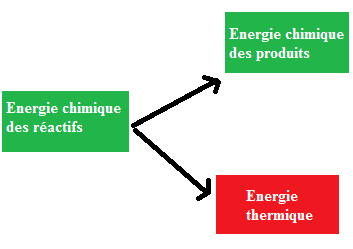
Toutes les espèces chimiques possèdent une forme d'énergie appelée énergie chimique;
Au cours de la transformation chimique une partie de cette énergie est transformée en énergie thermique
Bilan énergétique
3)Activités
 |
|

|

|
3S 18/01/17



